上海市静安区2017-2018学年高考理综-化学二模考试试卷
试卷更新日期:2018-06-13 类型:高考模拟
一、单选题
-
1. 下列过程不涉及化学变化的是( )A、用氨气做制冷剂 B、用氢氧化铝治疗胃酸过多 C、用糯米酿制甜酒 D、用食醋除去水壶中的水垢2. 2017年9月美俄科学家利用计算机模拟设计出密度比水还小的超轻晶体铝,这种晶体铝属于( )A、电解质 B、有机物 C、单质 D、化合物3. 属于同位素的两种微粒是( )A、H2和D2 B、2He和3He C、CH4和C2H6 D、O2和O34. 有关化学用语的表示中正确的是( )A、羟基电子式
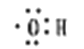 B、S2-的结构示意图
B、S2-的结构示意图  C、乙烯的结构简式CH2CH2
D、原子核内有20个中子的氯原子
5. 属于极性分子的是( )A、CO2 B、H2O C、CCl4 D、N26. 下列过程的热效应属于吸热的是( )A、碘蒸气的凝华 B、化学反应中化学键的形成 C、铝热反应 D、氯化铵的水解7. 有关性质的比较中,不能用元素周期律解释的是( )A、热稳定性:HCl>HBr B、金属性:Mg>Be C、碱性:KOH>Ca(OH)2 D、酸性:H2SO4>HClO8. 两种物质所含化学键种类完全相同,晶体类型也相同的是( )A、NaCl和HCl B、NaOH和Na2O C、C3H8和H2O2 D、SO2和SiO29. 将已除去氧化膜的镁条投入到盛有稀盐酸的敞口容器中,产生H2的速率v与时间t的关系如下图所示,其中影响AB段速率的主要因素是( )
C、乙烯的结构简式CH2CH2
D、原子核内有20个中子的氯原子
5. 属于极性分子的是( )A、CO2 B、H2O C、CCl4 D、N26. 下列过程的热效应属于吸热的是( )A、碘蒸气的凝华 B、化学反应中化学键的形成 C、铝热反应 D、氯化铵的水解7. 有关性质的比较中,不能用元素周期律解释的是( )A、热稳定性:HCl>HBr B、金属性:Mg>Be C、碱性:KOH>Ca(OH)2 D、酸性:H2SO4>HClO8. 两种物质所含化学键种类完全相同,晶体类型也相同的是( )A、NaCl和HCl B、NaOH和Na2O C、C3H8和H2O2 D、SO2和SiO29. 将已除去氧化膜的镁条投入到盛有稀盐酸的敞口容器中,产生H2的速率v与时间t的关系如下图所示,其中影响AB段速率的主要因素是( ) A、H+的浓度 B、Cl-的浓度 C、溶液的温度 D、体系的压强10. 某有机物加氢反应后生成
A、H+的浓度 B、Cl-的浓度 C、溶液的温度 D、体系的压强10. 某有机物加氢反应后生成 ,该有机物可能是( ) A、乙醛的同系物 B、戊醛的同分异构体 C、丙醇的同系物 D、丁醇的同分异构体11. ClO2是一种高效水处理剂,实验室通过以下反应制得ClO2: 2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O,关于此反应的说法正确的是( )A、KClO3发生化合价降低,失电子 B、反应中H2SO4体现了酸性和强氧化性 C、反应中H2C2O4被氧化 D、产物中Cl与C化合价相同,因而氧化性一样强12. 在pH=13的某溶液中存在大量的Na+、ClO-、NO3- , 该溶液还可能大量存在的离子是( )A、NH4+ B、CO32- C、HCO3- D、Al3+13. 将下列物质溶于水,能促进水的电离的是( )A、NaHSO4 B、Na2CO3 C、SO2 D、NaOH14. 实验室以石墨为电极电解饱和食盐水的装置如图所示,下列判断正确的是( )
,该有机物可能是( ) A、乙醛的同系物 B、戊醛的同分异构体 C、丙醇的同系物 D、丁醇的同分异构体11. ClO2是一种高效水处理剂,实验室通过以下反应制得ClO2: 2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O,关于此反应的说法正确的是( )A、KClO3发生化合价降低,失电子 B、反应中H2SO4体现了酸性和强氧化性 C、反应中H2C2O4被氧化 D、产物中Cl与C化合价相同,因而氧化性一样强12. 在pH=13的某溶液中存在大量的Na+、ClO-、NO3- , 该溶液还可能大量存在的离子是( )A、NH4+ B、CO32- C、HCO3- D、Al3+13. 将下列物质溶于水,能促进水的电离的是( )A、NaHSO4 B、Na2CO3 C、SO2 D、NaOH14. 实验室以石墨为电极电解饱和食盐水的装置如图所示,下列判断正确的是( ) A、通电使氯化钠发生电离 B、A电极上发生还原反应 C、B电极上有Cl2产生 D、通电一段时间后,阴极区pH上升15. 下列图示的实验设计能达到相应实验目的的是( )A、检验溴乙烷消去的产物
A、通电使氯化钠发生电离 B、A电极上发生还原反应 C、B电极上有Cl2产生 D、通电一段时间后,阴极区pH上升15. 下列图示的实验设计能达到相应实验目的的是( )A、检验溴乙烷消去的产物 B、检验FeCl3溶液中是否混有Fe2+
B、检验FeCl3溶液中是否混有Fe2+ C、检验亚硫酸钠溶液是否变质
C、检验亚硫酸钠溶液是否变质  D、验证钢铁的析氢腐蚀
D、验证钢铁的析氢腐蚀  16. 关于C、N、S等非金属元素及其化合物的说法错误的是( )A、它们都能以游离态存在于自然界中 B、二氧化硫、氮氧化物的任意排放会形成酸雨 C、浓硫酸可干燥CO2、SO2、H2S 等气体,但不能干燥NH3 D、加热条件下,碳、硫单质都能与浓硝酸、浓硫酸发生反应17. 已知C2H2 (g) + O2 (g) → 2CO2 (g) + H2O (g)+1256 kJ,下列说法正确的是( )A、1 份乙炔完全燃烧可放热1256 kJ B、反应中乙炔做还原剂、被还原 C、乙炔完全燃烧时,生成2 mol液态水,所放热量小于2512 kJ D、若有10 mol电子发生转移,则需消耗2.5 mol O218. 小苏打溶液水解的离子方程式书写正确的是( )A、HCO3-+H+→H2CO3 B、HCO3-+ H2O H2CO3+ OH- C、CO32-+ H2O HCO3-+ OH- D、HCO3-+ H2O CO32-+ H3O+19. 实验室用海带提取碘的操作过程中,所选仪器错误的是( )
16. 关于C、N、S等非金属元素及其化合物的说法错误的是( )A、它们都能以游离态存在于自然界中 B、二氧化硫、氮氧化物的任意排放会形成酸雨 C、浓硫酸可干燥CO2、SO2、H2S 等气体,但不能干燥NH3 D、加热条件下,碳、硫单质都能与浓硝酸、浓硫酸发生反应17. 已知C2H2 (g) + O2 (g) → 2CO2 (g) + H2O (g)+1256 kJ,下列说法正确的是( )A、1 份乙炔完全燃烧可放热1256 kJ B、反应中乙炔做还原剂、被还原 C、乙炔完全燃烧时,生成2 mol液态水,所放热量小于2512 kJ D、若有10 mol电子发生转移,则需消耗2.5 mol O218. 小苏打溶液水解的离子方程式书写正确的是( )A、HCO3-+H+→H2CO3 B、HCO3-+ H2O H2CO3+ OH- C、CO32-+ H2O HCO3-+ OH- D、HCO3-+ H2O CO32-+ H3O+19. 实验室用海带提取碘的操作过程中,所选仪器错误的是( )选项
操作
所选仪器
A
称取3 g左右的干海带
托盘天平
B
灼烧干海带至完全变成灰烬
烧杯
C
过滤煮沸后的海带灰与水的混合液
漏斗
D
用四氯化碳从氧化后的海带灰浸取液中提取碘
分液漏斗
A、A B、B C、C D、D20. 有关实验室制备乙酸乙酯和乙酸丁酯的描述错误的是( )A、两反应均需使用浓硫酸、乙酸 B、过量乙酸可提高1-丁醇的转化率 C、制备乙酸乙酯时乙醇应过量 D、提纯乙酸丁酯时,需过滤、洗涤等操作二、综合题
-
21. I.人类能够有效利用氮气的主要途径是合成氨,生产化学肥料等。
完成下列填空:
(1)、氮原子核外电子排布式为 , 其最外层有种运动状态不同的电子;氮气的电子式为;氨气分子的空间构型是。(2)、工业上常用醋酸亚铜氨溶液来吸收含有大量N2的高炉气体系中的CO,从而实现CO和N2的分离,反应的化学方程式如下:CH3COOCu(NH3)2 (aq) + CO(g) CH3COOCu(NH3)2·CO(aq) + Q(Q>0),该反应的化学平衡常数表达式K=;欲使K值变大,可采取的措施是。吸收CO后的溶液经过适当处理又可以重新生成醋酸亚铜氨,可采取的适当处理措施有
(选填序号)。
a.适当升高温度
b.适当降低温度
c.增大压强
d.减小压强
(3)、消除NH3对水体污染的重要方法是在一定条件下向水体中加入适量NaOH,这样能使NH3的脱除率增大,试用平衡移动原理解释其原因。(4)、某研究小组用200mL 1.5mol/L K2CO3溶液吸收了3.36L 的CO2(标准状况)形成富液,碳酸钾溶液吸收CO2的离子反应方程式为 , 该富液中的溶质是(填化学式),各离子的浓度关系正确的是。a.c(K+) + c(H+) = 2c(CO32-) +c(HCO3-) +c(OH-)
b.3c(K+)=4 c(CO32-)+4 c(HCO3-)+4c(H2CO3)
c.c(K+)>c(OH-)>c(HCO3-)>c(CO32-)>c(H+)
22. X、Y、Z、M、W、Q、R是7种短周期元素,其原子半径及主要化合价如下:元素代号
X
Y
Z
M
W
Q
R
原子半径/nm
0.186
0.143
0.104
0.099
0.070
0.066
0.032
主要化合价
+1
+3
+6,﹣2
+7,﹣1
+5,﹣3
﹣2
+1
完成下列填空:
(1)、上述元素中,金属性最强的在周期表中的位置是;X、Y、Q各自形成的简单离子中,离子半径由大到小的顺序是(填离子符号)。W和R按原子个数比1﹕4构成的阳离子所含的化学键是。
(2)、表中所列4种第三周期元素的最高价氧化物的水化物碱性最弱的是(填化学式),其电离方程式为。
(3)、M与Z相比,非金属性较强的是(填元素名称),请从原子结构的角度说明理由。(4)、在稀硫酸中,KMnO4和H2O2能发生氧化还原反应,反应方程式如下: KMnO4+
KMnO4+  H2O2+
H2O2+  H2SO4 →
H2SO4 →  K2SO4+
K2SO4+  MnSO4+
MnSO4+  O2↑+
O2↑+  H2O
H2O请配平 , 当有0.5 mol H2O2参加此反应,电子转移的个数为。
23. 晶须是由高纯度单晶生长而成的微纳米级的短纤维,工业应用的晶须主要是在人工控制条件下合成。碳酸镁晶须(MgCO3·nH2O,n = 1~5的整数)广泛应用于冶金、耐火材料及化工产品等领域。制取碳酸镁晶须的步骤如图:

完成下列填空:
(1)、步骤1必须将反应的温度控制在50℃,较好的加热方法是;氨水、硫酸镁、碳酸氢铵三者反应,除生成MgCO3·nH2O沉淀外,同时生成的产物还有。(2)、步骤2是、洗涤,检验沉淀A已洗涤干净的方法是。为测定碳酸镁晶须产品中n的值,某兴趣小组设计了如下装置,并进行了三次实验。(不考虑稀盐酸的挥发性)
 (3)、装置A中盛放的溶液是。装置D中盛放的固体是 , 其作用是。(4)、若三次实验测得每1.000g碳酸镁晶须产生的CO2平均值为a mol,则n值为(用含a的代数式表达)。(5)、下列选项中,会造成实验结果偏大的是。 (选填序号)
(3)、装置A中盛放的溶液是。装置D中盛放的固体是 , 其作用是。(4)、若三次实验测得每1.000g碳酸镁晶须产生的CO2平均值为a mol,则n值为(用含a的代数式表达)。(5)、下列选项中,会造成实验结果偏大的是。 (选填序号)①实验开始,未先通空气,即称量装置C; ②B中反应结束后,没有继续通空气;
③缺少装置A; ④缺少装置D;
⑤装置B中稀盐酸的滴加速率过快; ⑥装置C中的NaOH溶液浓度过大。
24. 有机物D的结构简式: ,学名肉桂酸,又名β-苯丙烯酸,主要用于香精香料、食品添加剂、医药工业、美容、农药、有机合成等方面,其合成路线(部分反应条件略去)如下所示:
,学名肉桂酸,又名β-苯丙烯酸,主要用于香精香料、食品添加剂、医药工业、美容、农药、有机合成等方面,其合成路线(部分反应条件略去)如下所示:
已知: ⅰ CH3CH=CH2 CH3CHO + HCHO;
ⅱ RCHO


完成下列填空:
(1)、C中含氧官能团名称是 , E的结构简式为。(2)、反应②的反应类型是 , A的名称是。(3)、反应①发生所需的试剂是。反应⑥的化学方程式为。(4)、D的分子式是 , 与D具有相同官能团的同分异构体有多种,其中一种的结构简式为。
(5)、设计一条以溴乙烷为原料合成乳酸( )的路线(其它试剂任选,合成路线常用的表示方式为:A B 目标产物)。。
)的路线(其它试剂任选,合成路线常用的表示方式为:A B 目标产物)。。