2016-2017学年福建省漳州市长泰县九年级上学期期中化学试卷
试卷更新日期:2017-01-05 类型:期中考试
一、选择题
-
1. 下列变化中,属于化学变化的是( )A、蜡烛燃烧 B、冰块融化 C、香水挥发 D、绞碎花生2. 夏天从冰箱中拿出一瓶饮料,放在空气中,饮料外壁会潮湿,说明空气中含有( )A、氧气 B、二氧化碳 C、水蒸气 D、氮气3. 下列物质中,含有氧分子的是( )A、雾霾 B、空气 C、二氧化碳 D、过氧化氢4. 将密封的方便面从平原带到高原时,包装袋鼓起,是因为袋内气体分子( )A、体积增大 B、质量变大 C、个数增多 D、间隔增大5. 下关于氧气的说法中错误的是( )A、氧气能支持燃烧,可作燃料 B、空气成分中氧气约占总体积的21% C、物质与氧气发生的反应都是氧化反应 D、水中的生物是依靠微溶于水中的氧气而生存6. 下列实验操作正确的是( )A、
 B、
B、 C、
C、 D、
D、 7. 豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指( )A、原子 B、分子 C、元素 D、单质8. 下列做法不合理的是( )A、用燃着的木条区分空气和氮气 B、滴加液体时,滴管的尖端不能触及已加过其它试剂的试管内壁 C、蒸发时用玻璃棒搅拌的目的是防止局部温度过高造成液滴飞溅 D、振荡试管时,用手掌紧握试管,同时拇指堵住试管口,上下晃动9. 常温常压下,下列物质不适宜用物理性质区分的是( )A、铜和铝 B、白酒和白醋 C、氧气和二氧化碳 D、汞(俗称水银)和铁10. 下列有关原子结构的说法中,正确的是( )A、碳、氢、氧的原子核都是由质子和中子构成的 B、氯原子的结构示意图为
7. 豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指( )A、原子 B、分子 C、元素 D、单质8. 下列做法不合理的是( )A、用燃着的木条区分空气和氮气 B、滴加液体时,滴管的尖端不能触及已加过其它试剂的试管内壁 C、蒸发时用玻璃棒搅拌的目的是防止局部温度过高造成液滴飞溅 D、振荡试管时,用手掌紧握试管,同时拇指堵住试管口,上下晃动9. 常温常压下,下列物质不适宜用物理性质区分的是( )A、铜和铝 B、白酒和白醋 C、氧气和二氧化碳 D、汞(俗称水银)和铁10. 下列有关原子结构的说法中,正确的是( )A、碳、氢、氧的原子核都是由质子和中子构成的 B、氯原子的结构示意图为 ,反应中若得到一个电子即变成氯离子(Cl﹣)
C、质子和中子的相对原子质量都约等于1,每个质子、中子都带一个单位正电荷
D、毒大米中镉(Cd)超标主要的危害是肾功能,镉核电荷数48,则其质子和中子数都是48
11. 下列对分子、原子、离子的认识不正确的是( )A、水、氯化钠、铜都是由分子构成 B、相同的原子可以构成不同的分子 C、装有空气的气球容易被压缩是因为气体分子间间隔较大 D、H2O和H2O2的化学性质存在差异,是因为构成物质的分子不同12. 对于H﹣、H、H+三种粒子,下列说法正确的是( )A、它们的化学性质相同 B、它们的质子数相同 C、它们粒子的名称相 D、它们的核外电子层结构相同13. 下列实验操作与所选择的仪器正确的是( )A、盛装固体药品﹣﹣细口瓶 B、取用硫磺粉末﹣﹣镊子 C、取用少量液体﹣﹣滴管 D、将试管固定在铁架台上﹣﹣试管夹14. 胆矾是一种蓝色晶体,化学式为CuSO4•5H2O,胆矾受热时容易分解而成为白色的CuSO4;工业上精炼铜、镀铜等都要应用胆矾,上述对胆矾的描述中,没有涉及的是( )A、物理性质 B、化学性质 C、制法 D、用途15. 实验室制取氧气的过程,大致分为以下六个主要操作:
,反应中若得到一个电子即变成氯离子(Cl﹣)
C、质子和中子的相对原子质量都约等于1,每个质子、中子都带一个单位正电荷
D、毒大米中镉(Cd)超标主要的危害是肾功能,镉核电荷数48,则其质子和中子数都是48
11. 下列对分子、原子、离子的认识不正确的是( )A、水、氯化钠、铜都是由分子构成 B、相同的原子可以构成不同的分子 C、装有空气的气球容易被压缩是因为气体分子间间隔较大 D、H2O和H2O2的化学性质存在差异,是因为构成物质的分子不同12. 对于H﹣、H、H+三种粒子,下列说法正确的是( )A、它们的化学性质相同 B、它们的质子数相同 C、它们粒子的名称相 D、它们的核外电子层结构相同13. 下列实验操作与所选择的仪器正确的是( )A、盛装固体药品﹣﹣细口瓶 B、取用硫磺粉末﹣﹣镊子 C、取用少量液体﹣﹣滴管 D、将试管固定在铁架台上﹣﹣试管夹14. 胆矾是一种蓝色晶体,化学式为CuSO4•5H2O,胆矾受热时容易分解而成为白色的CuSO4;工业上精炼铜、镀铜等都要应用胆矾,上述对胆矾的描述中,没有涉及的是( )A、物理性质 B、化学性质 C、制法 D、用途15. 实验室制取氧气的过程,大致分为以下六个主要操作:①点燃酒精灯,给试管加热②熄灭酒精灯③检查装置的气密性④将高锰酸钾装入试管里,试管口放一小团棉花,用带导管的胶塞塞紧,并将它固定在铁架台上⑤用排水法收集氧气⑥将导管从水中取出.正确的操作顺序是( )
A、④①③⑤⑥② B、①③④⑤⑥② C、④①③⑤②⑥ D、③④①⑤⑥②二、非选择题
-
16. 有限的元素可组成种类繁多的物质.请选择下表中的元素回答下列3个问题.
元素名称
氢
碳
氧
铁
(1)、请用化学式(符号)表示(每空只写一种):①只含一种元素的气体(常温下) ②一种常见的液体(常温下)
③生物体中含量最高的元素 ④一种常见的阳离子
(2)、某固体完全燃烧时生成的气体能使澄清的石灰水变浑浊,该反应式为 .(3)、若某元素的单质A在另一种元素的单质B中燃烧时,火星四射,生成黑色固体,则该黑色固体的化学式(符号) .17. 如表为元素周期表中某一周期元素的原子结构示意图.请回答下列问题: (1)、表中磷原子的核电荷数X= , 磷元素属于元素(填“金属”或“非金属”)(2)、表中具有相对稳定结构的元素是 .(3)、在化学反应中,每个铝原子失去个电子形成铝离子.(4)、上述元素在周期表中处于同一横行叫做第周期,它们的共同点是 .18. 某研究性学习小组用如图装置进行镁条在空气中烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.
(1)、表中磷原子的核电荷数X= , 磷元素属于元素(填“金属”或“非金属”)(2)、表中具有相对稳定结构的元素是 .(3)、在化学反应中,每个铝原子失去个电子形成铝离子.(4)、上述元素在周期表中处于同一横行叫做第周期,它们的共同点是 .18. 某研究性学习小组用如图装置进行镁条在空气中烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.
(1)、燃烧、冷却后打开止水夹,水能进入集气瓶中的原因是: .(2)、如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的 %.现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出与镁发生反应的气体除了氧气外,还一定有参与反应.(3)、【查阅资料】镁条在氮气中能燃烧,产物为黄绿色的氮化镁(Mg3N2)固体.请写出镁条在氮气中燃烧的化学反应式 .
19. 某同学对金属钠做了如下实验:用镊子从煤油中取出一块金属钠,用小刀切下一小块,切口呈银白色金属光泽,但光泽瞬间消失变暗,这是因为钠迅速与空气中的氧气反应生成氧化钠所致.将一小块钠投入水中,钠会漂浮于水面,同时与水发生剧烈反应,随即熔化成一个闪亮的小球,在水面上急速游动,钠逐渐减小直到完全消失.请分析以上实验现象,归纳出金属钠的有关性质:(1)、物理性质(小结出四点) , , , .(2)、化学性质:常温下能与反应;常温下还能与反应.20. 关于氧气的探究实验.化学兴趣小组的同学用下图装置进行实验,实验步骤见表,
 (1)、请填空:
(1)、请填空:实验步骤
简答
(1)称取3g氯酸钾后与少量二氧化锰混合再装入装置①的试管中
装置①的试管中发生反应式:
①
(2)加热试管一段时间后,用橡皮管连接a、b.
刚开始加热时,排出的气体不宜立即收集,原因是: ②
(3)当装置②中水面不再下降,断开a,b,移去酒精灯,将装置②中的集气瓶密封,并贴上标签备用.
(4)读取量筒里水的体积数并记录.
读数时视线必须与凹液面的 ③ 保持水平.
在理解上述实验的基础上,请你归纳本实验的目的:(不超过20个字) ④ .
(2)、我们了解到常见制取氧气的方法有如图所示的四种:
请回答问题:
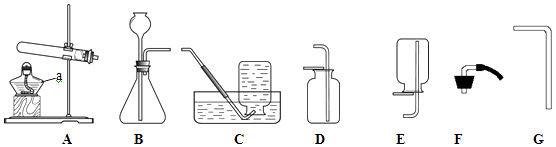
①工业制取氧气的方法是(填“甲、乙、丙、丁”);下图标有字母“a”的仪器名称是 .
②用甲方法制取并收集氧气时,你将选用下图装置中的 , 若说明集气瓶中已充满氧气,反应式为
 (3)、某化学兴趣小组的同学,利用乙方法制取氧气,探究如下.
(3)、某化学兴趣小组的同学,利用乙方法制取氧气,探究如下.①把过氧化氢溶液缓缓加入盛有二氧化锰的容器中制取并用排气法收集氧气,完成该实验你所选用的仪器有(填图中字母),写出化学反应式 , 该反应叫做;以上操作与“把二氧化锰加入盛有过氧化氢溶液的试管中制氧气”相比的优点是 .
②该小组继续探究“红砖粉末是否可以作为过氧化氢分解反应的催化剂?”实验如下:
a.分别向两支试管中加入相同的过氧化氢溶液,其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体导出通入水中比较产生气泡的快慢,结果发现加入红砖粉末的试管中反应较快.
b.将反应较快的试管内固体过滤出来,洗涤、烘干、称量.
c.用称量后的固体重复步骤a的实验,现象与步骤a完全相同.
请回答:步骤a中除了选用试管外,还用到上面的仪器(填字母).步骤c的实验目的是 . 该小组学生认为上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为实验还缺少一个步骤,请指出该步骤是 .