2018年广东省中考化学冲刺卷(一)
试卷更新日期:2018-06-04 类型:中考模拟
一、单选题
-
1. 下列事例中属于化学变化的是( )A、活性炭净水 B、蒸馏水获取淡水 C、以葡萄为原料酿酒 D、酒精挥发2. 下列不是合金的是( )A、生铁 B、铁锈 C、青铜 D、焊锡3. 2015年8月,天津一集装箱码头发生危化品大爆炸,再次敲响了人们对危化品管理的警钟,实验室常备的氢氧化钠属于危化品,你认为其包装箱上应贴的标识是( )
A、 B、
B、 C、
C、 D、
D、 4. 化学与人类的生活密切相关.下列对化学知识的应用归纳完全正确的一组是( )
4. 化学与人类的生活密切相关.下列对化学知识的应用归纳完全正确的一组是( )A.化学与生活
B.化学与安全
①用活性炭包可吸附汽车内的异味
②用洗涤剂可以洗掉衣服和餐具上的油污
①炒菜时油锅着火可以用锅盖盖灭
②在室内放一盆水能防止煤气中毒
C.化学与资源
D.化学与健康
①煤、石油、天然气都是可再生能源
②我国试采可燃冰成功,为未来使用新能源
①烧烤食品营养丰富,可大量食物
②每天食用适量蔬菜,以补充维生素
A、A B、B C、C D、D5. 常温下,下列物质水溶液的pH<7的是( )A、KOH B、草木灰 C、生石灰 D、醋酸6. 下列化学用语,说法正确的是( )①2N ②Mg2+③ ④H2⑤
 A、①表示两个氮分子 B、②与⑤均表示镁离子 C、③表示一氧化碳中碳元素的化合价为+2 D、④表示2个氢原子7. 如图的实验设计不能实现其对应实验目的是( )A、
A、①表示两个氮分子 B、②与⑤均表示镁离子 C、③表示一氧化碳中碳元素的化合价为+2 D、④表示2个氢原子7. 如图的实验设计不能实现其对应实验目的是( )A、 测定空气中O2含量
B、
测定空气中O2含量
B、 检验氢气的纯度
C、
检验氢气的纯度
C、 探究燃烧的条件
D、
探究燃烧的条件
D、 证明密度:CO2>空气
8. 亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素由防癌、抗癌的作用,它在元素周期表的部分信息记原子结构示意图如图所示,下列说法不正确的是( )
证明密度:CO2>空气
8. 亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素由防癌、抗癌的作用,它在元素周期表的部分信息记原子结构示意图如图所示,下列说法不正确的是( )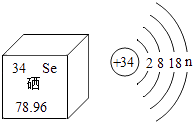 A、Na2SeO3中Se化合价为+4 B、n的值为6 C、Se是一种金属元素 D、Se的相对原子质量为78.969. 除去下列物质中的少量杂质(括号内为杂质),所选试剂正确的是( )A、CaCO3粉末(CaCl2粉末)﹣﹣水 B、CaO粉末[Ca(OH)2粉末]﹣﹣水 C、KCl溶液(KOH)﹣﹣稀硝酸 D、NaOH溶液(Na2CO3)﹣﹣稀盐酸10. 硝酸钾和氯化钾的溶解度曲线如图所示,下列叙述正确的是( )
A、Na2SeO3中Se化合价为+4 B、n的值为6 C、Se是一种金属元素 D、Se的相对原子质量为78.969. 除去下列物质中的少量杂质(括号内为杂质),所选试剂正确的是( )A、CaCO3粉末(CaCl2粉末)﹣﹣水 B、CaO粉末[Ca(OH)2粉末]﹣﹣水 C、KCl溶液(KOH)﹣﹣稀硝酸 D、NaOH溶液(Na2CO3)﹣﹣稀盐酸10. 硝酸钾和氯化钾的溶解度曲线如图所示,下列叙述正确的是( ) A、硝酸钾的溶解度一定大于氯化钾的溶解度 B、降低温度可使接近饱和的硝酸钾溶液变饱和 C、t℃时,硝酸钾和氯化钾两种溶液的溶质质量分数一定相等 D、60℃时,100g水中加入90g硝酸钾,充分搅拌,可得到硝酸钾的饱和溶液11. 下列实验操作、现象与结论一致的是( )
A、硝酸钾的溶解度一定大于氯化钾的溶解度 B、降低温度可使接近饱和的硝酸钾溶液变饱和 C、t℃时,硝酸钾和氯化钾两种溶液的溶质质量分数一定相等 D、60℃时,100g水中加入90g硝酸钾,充分搅拌,可得到硝酸钾的饱和溶液11. 下列实验操作、现象与结论一致的是( )序号
实验操作
现象
结论
A
向久置空气中的NaOH固体滴加盐酸
产生气泡
NaOH已部分变质
B
向某无色溶液滴入紫色石蕊试液
溶液变蓝
该溶液一定是碱溶液
C
将燃着的木条伸入盛满某气体的集气瓶中
木条熄灭
该气体是CO2
D
向碘化钾、稀硫酸和淀粉的混合液中加入某食用盐
溶液变蓝
该食用盐为加碘食盐
A、A B、B C、C D、D12.硝酸银受热时会发生如下反应:2AgNO3
 2Ag+2X↑+O2↑.根据质量守恒定律,推测X是( )A、N2O B、NO2 C、N2O5 D、NO13.
2Ag+2X↑+O2↑.根据质量守恒定律,推测X是( )A、N2O B、NO2 C、N2O5 D、NO13.下面对芝麻酱说明书的判断正确的是( )
 A、不含微量元素 B、不含糖类和油脂 C、婴儿最好不食用 D、钙铁含量低于豆腐和鸡蛋14. 下列图象能正确反应对应变化关系是( )
A、不含微量元素 B、不含糖类和油脂 C、婴儿最好不食用 D、钙铁含量低于豆腐和鸡蛋14. 下列图象能正确反应对应变化关系是( )



A.向一定质量的AgNO3溶液中滴加NaCl溶液
B.两份等体积5%的过氧化氢溶液,向其中一份加入少量二氧化锰
C.在恒温条件下,将饱和的KNO3溶液蒸发适量水
D.向氢氧化钠溶液中不断加水
A、A B、B C、C D、D二、填空题
-
15. 化学源于生活,生活中蕴含着许多化学知识.
(1)医用葡萄糖注射液中的溶剂是 .
(2)炒菜时锅里的油不慎着火,可用锅盖灭.其灭火原理是 .
(3)用加了洗涤剂的水清洗油腻的餐具,是利用洗涤剂的 (填“乳化”或“溶解”)功能.
(4)硬水洗涤衣物,既浪费肥皂也洗不净衣物,时间长了还会使衣物变硬.日常生活中用的方法来降低水的硬度.
16.如图为某化学反应在催化剂作用下的微观模拟示意图,其中“


 ”和“
”和“
 ”分别表示氢原子和氧原子.
”分别表示氢原子和氧原子.
 (1)、虚线框内应填的微观示意图是 (填序号).A、
(1)、虚线框内应填的微观示意图是 (填序号).A、
 B、
B、
 C、
C、
 D、
D、
 (2)、结合如图,从原子、分子的角度分析,在化学反应过程中,可分,而不能再分.(3)、请写出该反应的化学方程式 .17. 用98%的浓硫酸和蒸馏水配制19.6%的稀硫酸100g:
(2)、结合如图,从原子、分子的角度分析,在化学反应过程中,可分,而不能再分.(3)、请写出该反应的化学方程式 .17. 用98%的浓硫酸和蒸馏水配制19.6%的稀硫酸100g:(1)计算:所需定量的98%浓硫酸,还需要蒸馏水 g.
(2)量取混匀操作中所需玻璃仪器包括烧杯、量筒、胶头滴管和 .
(3)如果在量取98%浓硫酸时,仰读视数,其他操作都正确,则所配制出的稀硫酸的浓度会比19.6% .(“偏高”或“偏低”)
18. 氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途.(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是: .测量其溶液的pH时,可以 ,再用标准比色卡比较试纸显示的颜色,读取该溶液的pH.
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是: .
(3)用熟石灰来改良酸性土壤,反应的化学方程式是: (以土壤中含有硫酸为例).
(4)用熟石灰粉与草木灰(主要成分是K2CO3)按一定比例混合可制得高效环保农药“黑白粉”.使用时,选择在有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体.
①“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是 .
②“黑白粉”还可提供植物必需的营养素是 (填元素符号).
19. 在空格内简要说明下列错误操作可能造成的不良后果。错 误 操 作
不 良 后 果
⑴滴管取液后平放或倒置
⑵倾倒细口瓶中的液体时,标签没向着手心
⑶加热后的试管直接刷洗
⑷实验室剩余的药品放回原瓶
⑸用试管刷洗涤试管时,用力过猛
三、解答题
-
20. 如图中的物质为初中化学常见物质,他们之间的反应关系如图所示(“→”表示转化关系,“﹣”表示相互能反应,部分反应物、生成物或反应条件已略去).甲与A溶液反应得到浅绿色溶液;A、B发生中和反应,产物之一是厨房内常用的调味品;C常用于改良酸性土壤,且C的溶液与D的溶液反应可得到B;C的溶液与乙的溶液反应生成蓝色沉淀;乙与丙两种溶液反应生成两种不同颜色的沉淀.请回答:
 (1)、甲的化学式是;D的化学式是 .(2)、欲通过一步实验证明A、B是否恰好完全反应,需要向A、B反应后的溶液中加入的试剂是 .(3)、E→C反应的化学方程式是 .(4)、乙与丙两种溶液反应的化学方程式是 .21. 氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCl的制备流程如下:
(1)、甲的化学式是;D的化学式是 .(2)、欲通过一步实验证明A、B是否恰好完全反应,需要向A、B反应后的溶液中加入的试剂是 .(3)、E→C反应的化学方程式是 .(4)、乙与丙两种溶液反应的化学方程式是 .21. 氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCl的制备流程如下: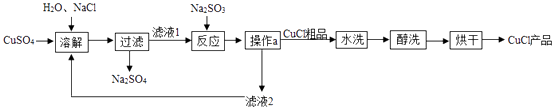 (1)、“滤液1”中除了Na+、SO42-外,还存在较多的离子是(写离子符号)。(2)、“反应”中发生的化学变化是2CuCl2+2Na2SO3=2CuCl↓+2NaCl+SO3 , 产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为。(3)、“操作a”的名称是。“醇洗”的目的是。(4)、本流程中可以循环利用的物质(水除外)是(写化学式)。(5)、320 g CuSO4与足量NaCl经上述制备流程,可生成的CuCl最多是g。
(1)、“滤液1”中除了Na+、SO42-外,还存在较多的离子是(写离子符号)。(2)、“反应”中发生的化学变化是2CuCl2+2Na2SO3=2CuCl↓+2NaCl+SO3 , 产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为。(3)、“操作a”的名称是。“醇洗”的目的是。(4)、本流程中可以循环利用的物质(水除外)是(写化学式)。(5)、320 g CuSO4与足量NaCl经上述制备流程,可生成的CuCl最多是g。四、实验探究题
-
22.
我国著名化学家侯德榜先生发明了“侯氏制碱法”,其原理中重要的一步是向饱和食盐水中先后通入足量NH3和CO2制备NaHCO3 , 化学方程式:NaCl+ NH3+CO2+H2O= NaHCO3↓+NH4Cl
某兴趣小组在实验室模拟该过程,请结合具体的步骤回答下列问题:
 (1)、I.气体制备
(1)、I.气体制备①二氧化碳气体制备实验室常采用石灰石与稀盐酸反应制备CO2 , 其化学方程式为。应选择的气体收集装置为(选填装置对应的字母)。
②氨气制备
实验室常用硫酸吸收氨气,防止污染空气,实验室制备NH3的反应原理为:Ca(OH)2(固)+2NH4Cl(固) CaCl2+2H2O+2NH3↑。现要制备并干燥NH3 , 所选装置的正确连接顺序为→(选择装置对应的字母)。实验室制备O2也可用上述制备NH3的发生装置,写出用该发生装置制备O2的化学方程式。
(2)、NaHCO3制备①根据表格中的溶解度数据,解释20℃产物中NaHCO3能够先从溶液中结晶析出的原因。
物质
NaHCO3
NH4Cl
溶解度/g(20℃)
9.6
37.2
②该过程中另一产物NH4Cl在农业生产中常被用作。
23. 某同学将一定质量的碳酸氢钠和稀硫酸混合,反应完全后(假设反应产生的气体全部逸出),对反应后溶液中溶质的成分进行如下探究:【实验用品】pH试纸、Zn片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液
【假设猜想】猜想一:硫酸钠 猜想二:硫酸钠、碳酸氢钠 猜想三:硫酸钠、硫酸
(1)、【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据现象或结论填空.实验方案
A
B
C
D
实验操作




实验现象
无气泡产生
试纸变色对照比色卡,pH<7
产生白色沉淀
实验结论
猜想三正确
猜想三正确
猜想三正确
【得出结论】猜想三正确.
(2)、【评价反思】老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在两处明显错误,分别是:①;② .
(3)、【总结提高】依据所给实验用品,你还有什么不同类方案确认猜想三是正确的,请你写出你的实验方案五、计算题
-
24. “舌尖上的中国”在央视上的热播让厨房再次成为人们施展厨艺的舞台.大多数厨师有个工作经验:炒菜时,又加料酒又加醋,可使菜变得香美可口,原因是醋中的乙酸与料酒之中的乙醇生成乙酸乙酯.如表中是几种常见的酯,请完成下列问题:
酯的名称
甲酸甲酯
甲酸乙酯
乙酸甲酯
乙酸乙酯
化学式
C2H4O2
C3H6O2
C3H6O2
X
(1)、甲酸甲酯(C2H4O2)中碳元素、氢元素、氧元素的质量比为;(2)、甲酸乙酯(C3H6O2)中碳元素的质量分数为(计算结果精确到0.1%);(3)、比较归纳是学习化学的重要方法,据表推测X额定化学式为 .25. 实验室欲测定一瓶标签破损的稀H2SO4的溶质质量分数.现取10g稀硫酸样品,将5%的NaOH溶液逐滴加到样品中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示.试回答: (1)、a点溶液中含有的离子有(2)、当pH=7时,消耗NaOH溶液中的NaOH的质量为 g.(3)、计算稀H2SO4的溶质质量分数.
(1)、a点溶液中含有的离子有(2)、当pH=7时,消耗NaOH溶液中的NaOH的质量为 g.(3)、计算稀H2SO4的溶质质量分数.